前言当地时间1月19日-21日,2023年美国临床肿瘤学会胃肠道肿瘤研讨会(ASCO GI)在旧金山拉开帷幕。在此次会议上,食管鳞状细胞癌(ESCC)领域中,我国多项安罗替尼联合治疗研究入选壁报(abstr 366、376、377、409),或将为ESCC患者带来新希望。医脉通编辑整理如下,以飨读者。366安罗替尼联合白蛋白紫杉醇和顺铂作为ESCC的新辅助治疗(NAT):一项单臂II期临床试验的最新结果背景新辅助放化疗与改善局部ESCC患者的总生存期(OS)、无病生存期(DFS)和病理完全缓解(pCR)相关。然而,对于ESCC患者,仍需探索更加可耐受的术前治疗方案。安罗替尼是一种多靶点抗血管生成抑制剂,在中国已证实其作为ESCC患者的二线单药治疗是有效且安全的(NCT02649361)。联合治疗方案或为一种可行的治疗策略。在2022 ASCO(e16015)和2022 ESMO(1252P)会议上,研究者已报道白蛋白紫杉醇、顺铂联合安罗替尼新辅助治疗ESCC的初步结果。此次会议上,研究者更新了结果。方法入组标准为临床II-III期、可行根治性切除的ESCC患者。计算样本量为62例,符合入组标准的患者于术前行安罗替尼(12mg,po,d1-14,q3w)、白蛋白紫杉醇(175mg/m2,iv,q3w)和顺铂(20mg/m2,iv,d1-3,q3w)两周期新辅助治疗。四周后,排除有禁忌症无法接受根治性手术的患者。主要研究终点为研究人员根据RECIST 1.1评估的可观缓解率(ORR),次要研究终点包括R0切除率、DFS、OS、疾病控制率(DCR)和安全性。结果从2021年4月至2022年9月,共入组40例符合标准的患者。其中,29例患者在接受两周期新辅助治疗后接受了手术,6例患者选择了其他治疗方案,5例患者仍在接受新辅助治疗。已接受手术的患者(n=29)纳入了分析。在最佳总体缓解评估中,ORR为86.2%(95%CI:68.3-96.1%),DCR为100.0%(95%CI:88.1-100.0%)。29例患者均行R0食管癌切除术。其中,4例(13.8%)患者pCR。截至2022年9月15日,中位DFS尚未达到。在入组的40例患者中,安全性资料显示,最常见的治疗相关紧急不良事件(TEAE)为胃肠道反应(80.0%)、肝损伤(15.0%)、恶心(12.5%)、低钾血症(10.0%)和骨髓抑制(10.0%)。2例(5.0%)患者发生3级TEAE,包括中性粒细胞减少(2.5%)和胃肠道反应(2.5%)。结论安罗替尼联合白蛋白紫杉醇和顺铂作为ESCC的新辅助治疗安全可行。376紫杉醇、顺铂联合安罗替尼作为晚期ESCC患者的一线治疗:一项多中心、单臂、开放标签II期临床试验的最新结果背景近二十年来,紫杉醇联合顺铂方案已成为晚期ESCC的一线标准治疗。近年来,PD-1抑制剂联合化疗作为ESCC的一线治疗疗效显著。安罗替尼是中国ESCC患者潜在的二线单药治疗药物。因此,本研究旨在探讨紫杉醇和顺铂联合安罗替尼作为一线治疗晚期ESCC的疗效和安全性。本研究已连续在2020 ESMO(Abs 1448)、2021 ASCO-GI Symposium(Abs 181)、2021 ASCO(e16013)、2021 ESMO(Abs 1805)和2022年ASCO-GI Symposium(Abs 315)上发表,此次报告更新结果。方法研究(NCT04063683)入组了既往未经治的转移性ESCC或局部晚期ESCC患者,行紫杉醇(135mg/m2,iv,q3w)和顺铂(60-75mg/m2,iv,d1-3,q3w)联合安罗替尼(10mg,po,d1-14,q3w)4-6周期作为起始治疗。对未出现PD的患者,采用安罗替尼单药维持治疗(10mg,po,d1-14,q3w),直至出现PD或出现不可耐受的毒性。根据RECIST 1.1评估肿瘤缓解,每两周期行CT检查。预定义样本量为47例。主要研究终点为PFS,次要研究终点包括安全性、ORR、DCR和缓解持续时间(DoR)。结果从2019年10月至2021年3月,共入组47例患者,其中46例纳入各方案分析集。最佳总体缓解为完全缓解(CR)4例(8.7%),部分缓解(PR)31例(67.4%),疾病稳定(SD)7例(15.2%),无法评估(NE)4例(8.7%)。ORR为76.1%(95%CI:61.2%-87.4%),DCR为91.3%(95%CI:79.2%-97.6%)。截至2022年1月,中位PFS和中位OS分别为8.38个月(95%CI:6.59-10.17)和18.53个月(95%CI:13.11-23.95)。此外,安全性资料显示该方案可耐受。常见的≥3级不良事件为中性粒细胞减少(17.0%)、骨髓抑
未来相关
未来相关文章,未来相关资讯,58hv关于未来的综合栏目,实时更新未来的咨询,未来的百科,未来的科普等等重要信息
决定未来设计方向,标致Inception概念车亮相CES,线条更加犀利
2023 CES电子消费展期间,标致Inception概念车首次亮相。新车基于标致BEV-by-design全新电动平台打造,虽然这款概念车后续将不会量产,但它的造型风格预计会应用......
中国经济的现状与未来,不同人群怎么看?
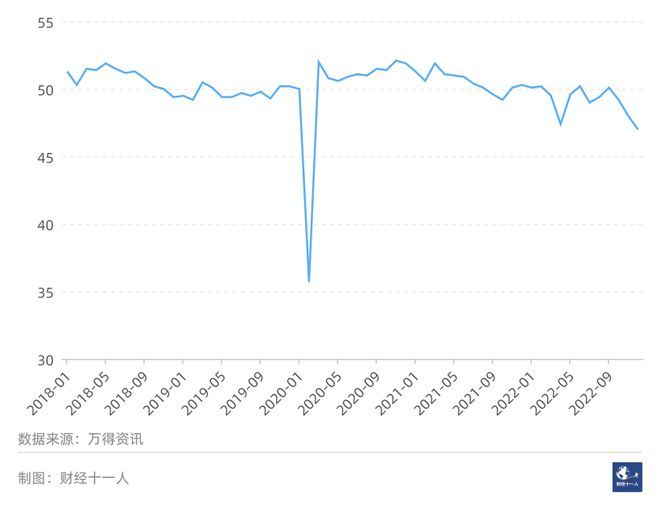
综合利用采购经理、城市储户、企业家、消费者多个人群对经济的感知,可以获得丰富的信息,有助于更全面地了解经济现状与未来文 | 刘建中 陈汐我们经常用各类经济......
2022年,我国人口总量首现负增长,减少85万人。人口数量由增转减与人口结构老龄化并存,已经成为我国经济社会发展的基本国情。南开大学经济学院教授、中国人口学......
【醍醐音】之汪颖教授:细数TNBC 2022治疗进展,看未来发展方向路在何方?
三阴性乳腺癌(TNBC)具有很强的异质性,尽管化疗仍是目前TNBC的主要治疗方案,但随着对分子生物学研究的不断深入,TNBC的分型逐渐被细化,并针对不同亚分型开发......
记者:蒋汉昆摄像:李梓晗翼虎投资董事长、投资总监余定恒,25年境内外证券投资及投行经历,对中国证券市场的发展历程具有独到而又深刻的理解,将价值投资与创新......
007未来座驾长这样!阿斯顿马丁DB12路试曝光,最快年底发布
近日,外媒在加油站拍到了一台覆盖着绿色伪装布的阿斯顿马丁DB11,而原型车辆贴纸的出现让人不得不怀疑,这其实是马上推出的下一代阿斯顿马丁DB12。从外观来看,......
未来三周有吉星护体,四大星座好运连连,财源滚滚,翻身富贵可期
未来三周有吉星护体,这四大星座好运连连,财源滚滚,未来收入翻番,翻身富贵可期金牛座金牛座很幸运,在生活中,他们经常会获得意想不到的收入。但是,金牛座的......
未来9天有财神庇佑,这三大星座实力兼备,注定多财多利
未来9天有财神庇佑,这三大星座坐拥好运,兼备实力,注定多财多利水瓶座水瓶座面对困难不会退缩,从来对自己的选择都拥有足够的信心。水瓶座做事总能够持之以恒......
未来8天好运停不下来,这几个星座马上就会迎来人生逆袭
未来8天横财连连,好运停不下来,这几个星座的财运抽中上上签,马上就会迎来人生逆袭双子座双子座的人生性聪明,他们精明,但是也足够大气。未来8天横财连连,好......
未来6天,这三大星座天天有好运,不仅正财给力,还有横财连连
未来6天,这三大星座天天有好运,不仅正财给力,还有横财连连,甚至能把钞票堆成山水瓶座水瓶座实力过人,做事从来都比看起来更加靠谱。他们脚踏实地,做事有头......
未来23天好运连连,这四大星座的所有梦想都有机会照进现实
未来23天好运连连,这四大星座注定行大运,添新喜,发大财,所有梦想都有机会照进现实双鱼座双鱼座完全可以被称为财富的搬运工,虽然他们的创造力不足,但是对财......
栏目推荐
-

再熬2周,四大生肖富贵满堂彩,工作有好运,好事成双
-

再熬2周,四大生肖家和万事兴,大显身手,兴旺发达
-

再熬2周,四大生肖好运连连,金玉满堂,越过越好
-

再熬2周,四大生肖大显身手,赚钱心里美,福气满满
-

再熬2周,四大生肖大显身手,福气满满,有钱有底气
-

再熬2周,四大生肖大展鸿图,顺风顺水,风调雨顺
-

再熬2周,四大生肖喜事连连,一帆风顺,家和万事兴
-

再熬2周,四大生肖命里财旺,贵人相助,富贵满堂彩
-

《舞力全开》国行版特别应援活动现已推出
-

再熬2周,四大生肖吉星高照,不缺好运,幸运无限
-

再熬2周,四大生肖兴旺发达,事业大吉,不缺机遇
-

再熬2周,四大生肖事业顺风顺水,不缺好运,收获意外惊喜
-

再熬2周,四大生肖事业有成,生意顺水行舟,福气满满
-

再熬2周,四大生肖事业有好运,好运连连,好运一触即发
-

再熬2周,四大生肖不缺好运,财富滚滚,鸿运当头
-

再熬29日,四大生肖大显身手,心想事成,大显身手
-

《胡闹搬家2》发售日确认 8月15日推出
-

再熬28天,四大生肖不缺机遇,走向人生巅峰,瑞气盈门
-

再熬27日,四大生肖收获大满贯,富贵满堂彩,鸿运连连
-

再熬27天,四大生肖金玉满堂,命中有锦鲤护航,贵人相助
-

再熬27天,四大生肖瑞雪兆丰年,有钱有底气,生活舒心惬意
-

《胡闹搬家 2》今年8月15日正式发售 立即加入成为F.A.R.T.一员
-

再熬24天,四大生肖收获意外惊喜,鸿运天降,越过越好
-

再熬23日,四大生肖欣欣向荣,好运连连,幸福美满