1月25日,美国食品药品监督管理局(FDA)批准tebentafusp-tebn用于HLA-A*02:01阳性不可切除或转移性葡萄膜黑色素瘤成人患者。3月4日,纳武利尤单抗联合含铂双药化疗获FDA批准用于可切除的非小细胞肺癌(NSCLC)成人患者的新辅助治疗。3月18日,纳武利尤单抗+relatlimab-rmbw复方制剂(Opdualag)获批用于不可切除或转移性黑色素瘤。7月14日,FDA批准克唑替尼用于治疗不可切除、复发或难治性ALK阳性炎性肌纤维母细胞瘤(IMT)成人或≥1岁的儿童。8月10日,capmatinib获批用于MET外显子14跳跃突变转移性NSCLC成人患者。8月11日,trastuzumab deruxtecan(DS-8201)获FDA加速批准用于既往接受过全身治疗的HER2突变不可切除或转移性NSCLC成人患者。9月21日,FDA加速批准selpercatinib扩展适应证,用于RET基因融合阳性局部晚期或转移性实体瘤患者。11月8日,FDA批准cemiplimab-rwlc联合铂类化疗用于无EGFR、ALK或ROS1突变晚期NSCLC成人患者。11月10日,FDA批准tremelimumab联合度伐利尤单抗和铂类化疗用于无EGFR或ALK驱动基因转移性NSCLC成人患者。12 月 9 日,FDA批准阿替利珠单抗用于不可切除或转移性腺泡状软组织肉瘤(ASPS)成人及2岁及以上儿童患者。12月12日, FDA加速批准adagrasib用于既往至少接受过一次全身治疗的KRAS G12C突变局部晚期或转移性NSCLC患者。1月25日2022年1月25日,FDA批准tebentafusp-tebn(一种双特异性融合蛋白),用于HLA-A*02:01阳性不可切除或转移性葡萄膜黑色素瘤成人患者。 此次获批主要基于IMCgp100-202 (NCT03070392)研究,这是一项针对 378例转移性葡萄膜黑色素瘤患者的随机、开放标签、多中心试验。入组患者随机分配(2:1)至tebentafusp药物组(252例)或由研究者选择的药物(帕博利珠单抗、伊匹木单抗或达卡巴嗪)对照组(126例)。Tebentafusp组静脉注射:首日20 mg,第8天30 mg,此后每周68 mg。其中前三剂为住院治疗,后续为门诊治疗。对照组按标准剂量和时间表进行治疗。出现疾病进展或不可接受的毒性反应时治疗中止。主要终点为总生存期(OS)。结果表明,tebentafusp组的疗效较对照组明显改善。Tebentafusp组中位OS为21.7个月,对照组为16.0个月;两组的中位PFS分别为3.3个月和2.9个月。Tebentafusp组和对照组分别有9%和5%的患者出现客观缓解,两组的疾病控制率(完全缓解,部分缓解,或疾病稳定12周)分别为46%和27%。Tebentafusp组最常见的不良事件是细胞因子释放综合征(89%)、皮疹(83%)、发热(76%)和瘙痒(69%)。Tebentafusp组和对照组3级及以上治疗相关不良事件的发生率分别为44%和17%。3月4日FDA批准纳武利尤单抗联合含铂双药化疗用于可切除NSCLC成人患者的新辅助治疗。此次获批主要基于CheckMate-816研究:一项随机、开放标签临床试验,旨在评估纳武利尤单抗联合化疗用于可切除、组织学证实为IB期(≥4cm)、II期或IIIA期NSCLC(AJCC/UICC分期标准)、可测量病灶(RECIST v1.1)患者的疗效。结果显示,纳武利尤单抗联合化疗组的中位无病生存期(EFS)为31.6个月(95%CI,30.2-未达到),而单化疗组的中位EFS为20.8个月(95%CI,14.0-26.7)。风险比为0.63(97.38%CI,0.43-0.91;p=0.0052)。纳武利尤单抗联合化疗组的pCR率为24%(95%CI,18.0-31.0),单化疗组的pCR率为2.2%(95%CI,0.6-5.6)。 详情点击:2022年3月18日FDA批准纳武利尤单抗+relatlimab-rmbw复方制剂用于≥12岁、不可切除或转移性黑色素瘤的成人和未成年患者。该批准基于随机(1:1)双盲II/III期研究RELATIVITY-047(NCT03470922)研究数据,该研究针对714例既往未经治疗的转移性或不可切除III/IV期黑色素瘤患者,对纳武利尤单抗+relatlimab-rmbw复方制剂的疗效和安全性进行了评估。结果显示,与纳武利尤单抗相比,复方制剂组的PFS表现出统计学意义上的改善(HR 0.75;95% CI,0.62~0.92;P=0.0055)。复方制剂组的中位无进展生存期(PFS)为10.1个月(95% CI,6.4~15.7),纳武利尤单抗组为4.6个
年度相关
年度相关文章,年度相关资讯,58hv关于年度的综合栏目,实时更新年度的咨询,年度的百科,年度的科普等等重要信息
批准情况简述1纳武利尤单抗联合化疗,以及纳武利尤单抗联合伊匹木单抗获批食管鳞状细胞癌(ESCC)一线治疗适应征2达拉非尼联合曲美替尼加速获批治疗BRAF V600E突变型不可切除或转移性实体瘤3度伐利尤单抗联合化疗获批局部晚期或转移性胆道癌(BTC)一线治疗适应征4塞普替尼加速获批治疗RET基因融合阳性局部晚期或转移性实体瘤5Futibatinib加速获批治疗既往接受过治疗、不可切除且存在FGFR2基因融合或重排的局部晚期或转移性肝内胆管癌6Tremelimumab与度伐利尤单抗获批不可切除肝细胞癌(HCC)的一线治疗适应征7FDA批准卡培他滨的药物标签更新012022年5月27日FDA批准纳武利尤单抗联合氟嘧啶和铂类化疗,以及纳武利尤单抗联合伊匹木单抗作为晚期或转移性食管鳞状细胞癌(ESCC)的一线治疗。该批准主要基于随机对照、开放标签、III期CheckMate-648研究,研究纳入970例既往未经治疗的不可切除晚期、复发性或转移性ESCC患者。患者被随机(1:1:1)分配接受以下治疗:纳武利尤单抗240 mg,d1和d15;5-FU 800 mg/m²,d1-5;顺铂80 mg/m²,d1;q4w;纳武利尤单抗3 mg/kg,q2w;伊匹木单抗1 mg/kg,q6w;5-FU 800 mg/m²,d1-5;顺铂80 mg/m²,d1;q4w;研究的主要疗效终点为总生存期(OS)和盲法独立中心审查(BICR)评估的无进展生存期(PFS)。结果显示,在总体人群中,与单纯化疗组相比,纳武利尤单抗+化疗组的OS获益显著(13.2个月 vs. 10.7个月;HR=0.74;95%CI,0.61-0.90;p=0.0021),纳武利尤单抗+伊匹木单抗组同样存在显著OS获益(12.8个月 vs. 10.7个月;HR=0.78;95%CI,0.65-0.95;p=0.0110)。在PD-L1评分≥1%的患者中,与单纯化疗组相比,纳武利尤单抗+化疗组(HR=0.54;95%CI,0.41-0.71;p<0.0001)和纳武利尤单抗+伊匹木单抗组(HR=0.64;95%CI,0.49-0.84;p=0.0010)依然存在显著的OS获益。研究中,纳武利尤单抗+化疗组最常见(≥20%)的不良反应包括恶心、食欲下降、疲劳、便秘、口腔炎、腹泻和呕吐,纳武利尤单抗+伊匹木单抗组最常见(≥20%)的不良反应包括皮疹、疲劳、发热、恶心、腹泻和便秘。方案的推荐用药剂量为:① 纳武利尤单抗240 mg q2w或 480 mg q4w,并联合氟嘧啶和含铂类化疗;② 纳武利尤单抗3 mg/kg q2w或360 mg q3w,联合伊匹木单抗1 mg/kg q6w。022022年6月22日FDA加速批准达拉非尼联合曲美替尼用于治疗存在BRAF V600E突变的不可切除或转移性实体瘤患者,患者为经既往治疗后疾病进展且无替代治疗方案的成人或≥6岁的儿童。值得注意的是,由于对BARF抑制剂存在内在耐药性,该方案并不适用于结直肠癌(CRC)患者,此外,达拉非尼不适用于BRAF野生型实体瘤患者。该加速批准基于BRF117019、NCI-MATCH、CTMT212X2101、COMBI-d、COMBI-v和BRF113928等多项研究,点击链接查看批准详情:。在美国国立综合癌症网络(NCCN)肝胆癌诊疗指南中,该治疗策略被推荐作为BRAF V600E突变型BTC二线治疗的可选策略;在NCCN胰腺癌诊疗指南中,该治疗策略被推荐作为BRAF V600E突变型患者一线治疗和二线治疗的可选策略。成人患者推荐的达拉非尼用药剂量为150 mg,口服,bid;曲美替尼2 mg,口服,qd。儿科患者推荐的用药剂量需基于体重,体重<26 kg的患者推荐剂量尚未确定。032022年9月2日FDA批准度伐利尤单抗联合吉西他滨和顺铂治疗局部晚期或转移性BTC成年患者。该批准基于随机、双盲、安慰剂对照、多区域III期TOPAZ-1研究,该研究纳入685例经组织学确诊的局部晚期不可切除或转移性BTC患者,患者既往未接受针对晚期疾病的全身治疗。纳入的患者中,肝内胆管癌占比为56%,胆囊癌占比为25%,肝外胆管癌占比为19%,患者随机(1:1)分配接受以下治疗:度伐利尤单抗1500 mg,d1;吉西他滨1000 mg/m², 顺铂25 mg/m²,d1和d8;q21d,最多8个周期;序贯度伐利尤单抗1500 mg,q4w;安慰剂1500 mg,d1;吉西他滨1000 mg/m², 顺铂25 mg/m²,d1和d8;q21d,最多8个周期;序贯安慰剂治疗q4w;度伐利尤单抗或安慰剂持续使用直至疾病进展或毒性不可接受。如果患者的临床病情稳定并存在临床获益,则允许在疾病进展之后接受由研究者决定的治疗。研究的主要疗效
乳腺癌12022年8月5日2022年8月5日,美国食品药品监督管理局(FDA)批准fam-trastuzumab deruxtecan nxki(DS-8201,T-DXd)用于治疗不可切除或转移性HER2低表达......
2023Wind星选理财师年度评选由中国金融信息服务行业领先企业Wind联合国际注册理财师协会的官方授权机构RFP(中国)重磅打造,旨在赋能中国财富管理行业发展,协......
12星座年度塔罗主题
2023年在数字学中跟7有关,7在塔罗牌中是由【战车】代表的,意味着2023年是坚守、适当采取行动和成就伟业的一年。但是你也要注意,你可能急躁地想在极短的时间内......
由中国经济传媒协会主办,新浪财经、第一财经联合承办的“中国梦杯•中国经济新闻人物——2022十大经济年度人物”颁奖盛典于2023年1月6日在北京正式举办。四位快......
2022年度豪华车销量榜,二线疲软,新能源车仍不是BBA的对手?
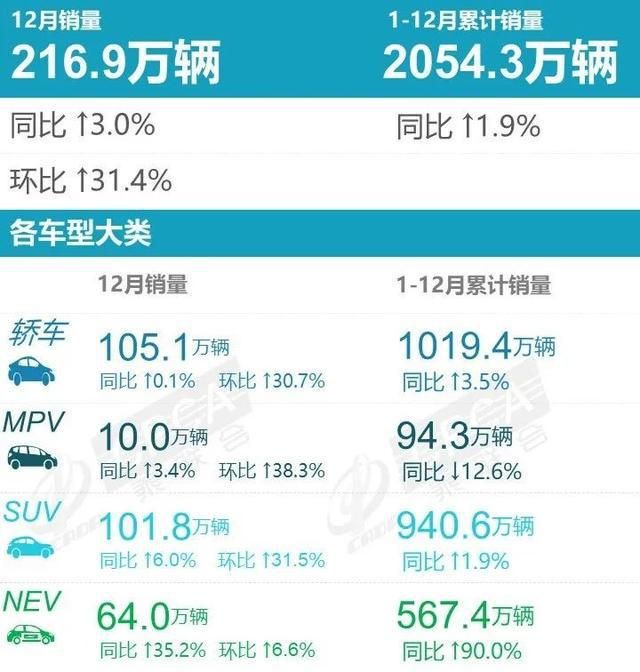
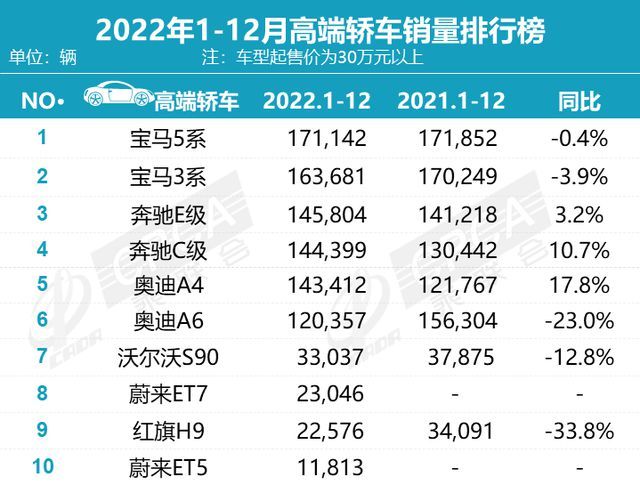
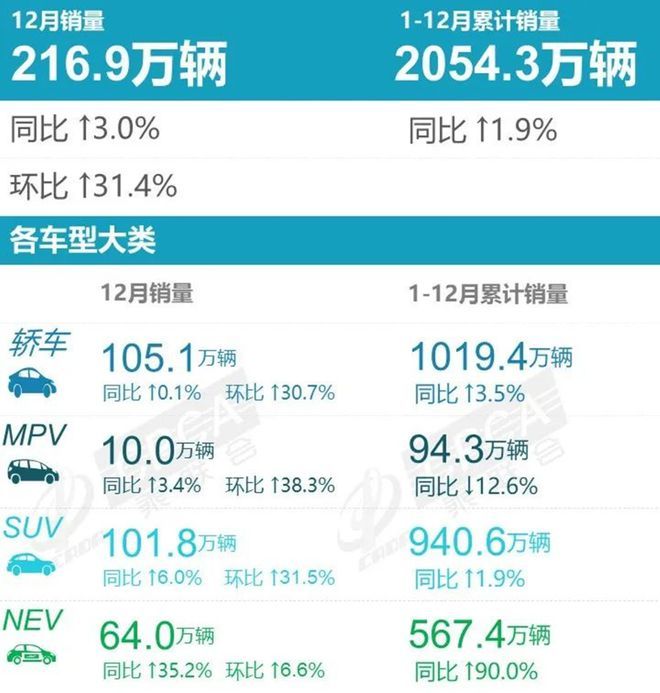
近日,乘联会公布了最新销量数据,2022年全年累计销量2054.3万辆,同比增长1.9%。大家比较关心的豪华车销量情况如何?我们一起来关注一下。2022年高端轿车销量榜......
2022年度豪华车销量榜,二线疲软,新能源车仍不是BBA的对手?
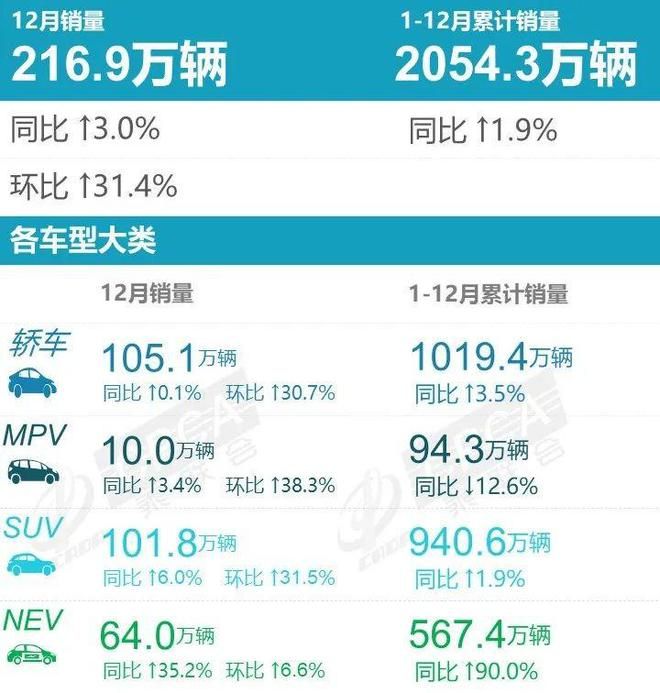
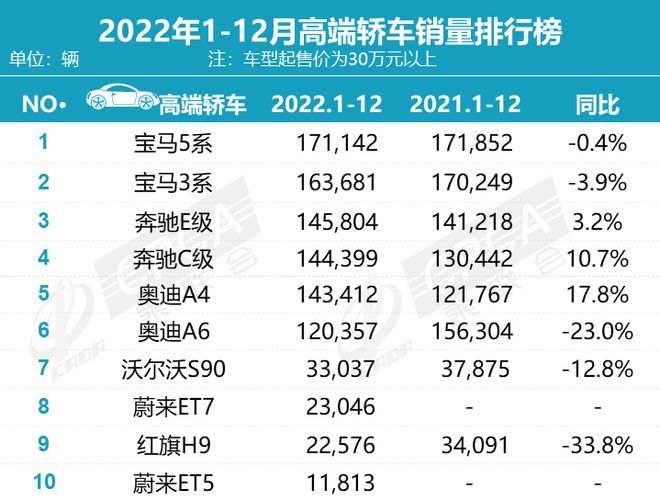
近日,乘联会公布了最新销量数据,2022年全年累计销量2054.3万辆,同比增长1.9%。大家比较关心的豪华车销量情况如何?我们一起来关注一下。2022年高端轿车销量榜......
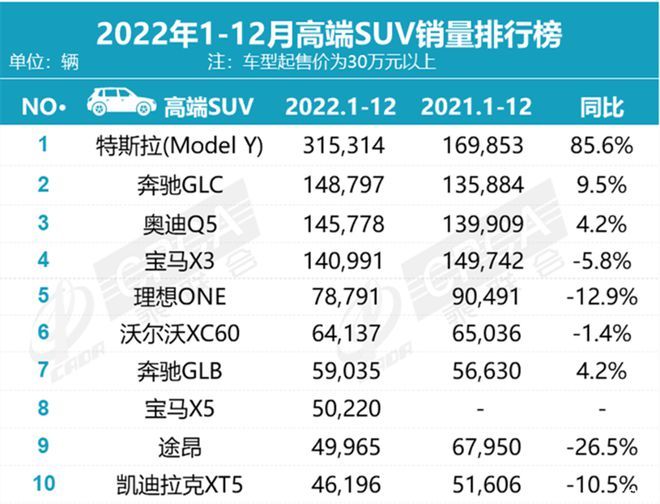
2022年度豪华车销量发布,国人最爱买这10款SUV,国产车仅这一款
如果说哪一个细分市场在国内市场基数和需求量最大,那一定还是轿车市场,根据中国汽车流通协会汽车市场研究分会(乘联会)最新零售销量数据统计:2022年国内狭义......
华夏时报(www.chinatimes.net.cn)记者 孙梦圆 于娜 北京报道2023年1月12日,在华夏时报社主办的第二届华夏大健康™产业高峰论坛上,2022年度金手杖奖获奖名单......
本报(chinatimes.net.cn)记者孙梦圆 于娜 北京报道2023年1月12日,在华夏时报社主办的第二届华夏大健康™产业高峰论坛上,2022年度金手杖奖获奖名单揭晓。诺辉......
本报(chinatimes.net.cn)记者王瑜 于娜 北京报道2023年1月12日,在华夏时报社主办的第二届华夏大健康™产业高峰论坛上,2022年度金手杖奖获奖名单揭晓。贝瑞基......
栏目推荐
-

再熬2周,四大生肖富贵满堂彩,工作有好运,好事成双
-

再熬2周,四大生肖家和万事兴,大显身手,兴旺发达
-

再熬2周,四大生肖好运连连,金玉满堂,越过越好
-

再熬2周,四大生肖大显身手,赚钱心里美,福气满满
-

再熬2周,四大生肖大显身手,福气满满,有钱有底气
-

再熬2周,四大生肖大展鸿图,顺风顺水,风调雨顺
-

再熬2周,四大生肖喜事连连,一帆风顺,家和万事兴
-

再熬2周,四大生肖命里财旺,贵人相助,富贵满堂彩
-

《舞力全开》国行版特别应援活动现已推出
-

再熬2周,四大生肖吉星高照,不缺好运,幸运无限
-

再熬2周,四大生肖兴旺发达,事业大吉,不缺机遇
-

再熬2周,四大生肖事业顺风顺水,不缺好运,收获意外惊喜
-

再熬2周,四大生肖事业有成,生意顺水行舟,福气满满
-

再熬2周,四大生肖事业有好运,好运连连,好运一触即发
-

再熬2周,四大生肖不缺好运,财富滚滚,鸿运当头
-

再熬29日,四大生肖大显身手,心想事成,大显身手
-

《胡闹搬家2》发售日确认 8月15日推出
-

再熬28天,四大生肖不缺机遇,走向人生巅峰,瑞气盈门
-

再熬27日,四大生肖收获大满贯,富贵满堂彩,鸿运连连
-

再熬27天,四大生肖金玉满堂,命中有锦鲤护航,贵人相助
-

再熬27天,四大生肖瑞雪兆丰年,有钱有底气,生活舒心惬意
-

《胡闹搬家 2》今年8月15日正式发售 立即加入成为F.A.R.T.一员
-

再熬24天,四大生肖收获意外惊喜,鸿运天降,越过越好
-

再熬23日,四大生肖欣欣向荣,好运连连,幸福美满